文章目录
1. 蛋白质结构
蛋白质结构 (protein structure) 是指蛋白质分子的空间结构。蛋白质主要由碳、氢、氧、氮等化学元素组成,是一类重要的生物大分子,所有蛋白质都是由 20种不同氨基酸 (amino acids) 连接形成的多聚体,在形成蛋白质后,这些氨基酸又被称为 残基 (residue)。
蛋白质和多肽之间的界限并不是很清晰,有人基于发挥功能性作用的结构域所需的残基数认为,若残基数少于40,就称之为 多肽 (polypeptide) 或 肽(peptide)。

要发挥生物学功能,蛋白质需要正确折叠为一个特定构型,主要是通过大量的 非共价相互作用 (non-covalent forces)(如氢键,离子键,范德华力和疏水作用)来实现;此外,在一些蛋白质(特别是分泌性蛋白质)折叠中,二硫键也起到关键作用。
蛋白质分子是由氨基酸首尾相连缩合而成的共价多肽链,但是天然蛋白质分子并不是走向随机的松散多肽链。每一种天然蛋白质都有自己特有的空间结构或称三维结构,这种三维结构通常被称为蛋白质的构象,即蛋白质的结构。
蛋白质的分子结构可划分为四级,以描述其不同的方面:
- 一级结构 (primary sequence):组成蛋白质多肽链的线性氨基酸序列。
- 二级结构 (secondary structure):依靠不同氨基酸之间的 C=O 和 N-H 基团间的氢键形成的稳定结构,主要为 α 螺旋(α-helix) 和 β 折叠(β-sheet)。
- 三级结构 (tertiary structure):通过多个二级结构元素在三维空间的排列所形成的一个蛋白质分子的三维结构。
- 四级结构 (quaternary structure):用于描述由不同多肽链(亚基 (subunit))间相互作用形成具有功能的蛋白质复合物分子。
1. 一级结构 (primary sequence)
蛋白质的 一级结构 (primary sequence) 就是蛋白质多肽链中氨基酸残基的排列顺序(sequence),也是蛋白质最基本的结构。它是由基因上遗传密码的排列顺序所决定的。各种氨基酸按遗传密码的顺序,通过肽键连接起来,成为多肽链,故肽键是蛋白质结构中的主键。

蛋白质分子的多肽链并非呈线形伸展,而是折叠和盘曲构成特有的比较稳定的空间结构。蛋白质的生物学活性和理化性质主要决定于空间结构的完整,因此仅仅测定蛋白质分子的氨基酸组成和它们的排列顺序并不能完全了解蛋白质分子的生物学活性和理化性质。例如球状蛋白质(多见于血浆中的白蛋白、球蛋白、血红蛋白和酶等)和纤维状蛋白质(角蛋白、胶原蛋白、肌凝蛋白、纤维蛋白等),前者溶于水,后者不溶于水,显而易见,此种性质不能仅用蛋白质的一级结构的氨基酸排列顺序来解释。
2. 二级结构 (secondary structure)
蛋白质的 二级结构 (secondary structure) 是指多肽链中主链原子的局部空间排布即构象,不涉及侧链部分的构象。
1. 肽键平面(或称酰胺平面, amide plane)
Pauling等人对一些简单的肽及氨基酸的酰胺等进行了X线衍射分析,从一个 肽键 (peptide bond) 的周围来看,得知:
(1)肽键中的C-N键长0.132nm,比相邻的N-C单键(0.147nm)短,而较一般C=N双键(0.128nm)长,可见,肽键中-C-N-键的性质介于单、双键之间,具有部分双键的性质,因而不能旋转,这就将固定在一个平面之内。
(2) 肽键的C及N周围三个键角之和均为360°,说明都处于一个平面上,也就是说六个原子基本上同处于一个平面,这就是肽键平面。肽链中能够旋转的只有α碳原子所形成的单键,此单键的旋转决定两个肽键平面的位置关系,于是肽键平面成为肽链盘曲折叠的基本单位。
(3) 肽键中的C-N既具有双键性质,就会有顺反不同的立体异构,已证实处于反位。
2. 蛋白质主链构象的结构单元
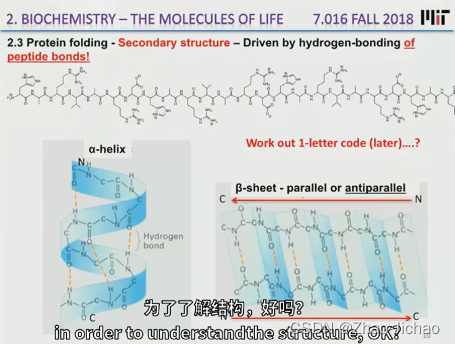
1)α-螺旋Pauling等人对α-角蛋白(α-keratin)进行了X线衍射分析,从衍射图中看到有0.5~0.55nm的重复单位,故推测蛋白质分子中有重复性结构,并认为这种重复性结构为α-螺旋(α-helix).
2)β-片层结构Astbury等人曾对β-角蛋白进行X线衍射分析,发现具有0.7nm的重复单位。如将毛发α-角蛋白在湿热条件下拉伸,可拉长到原长二倍,这种α-螺旋的X线衍射图可改变为与β-角蛋白类似的衍射图。说明β-角蛋白中的结构和α-螺旋拉长伸展后结构相同。两段以上的这种折叠成锯齿状的肽链,通过氢键相连而平行成片层状的结构称为β-片层(β-pleated sheet)结构或称β-折迭。
3. 三级结构 (tertiary structure)
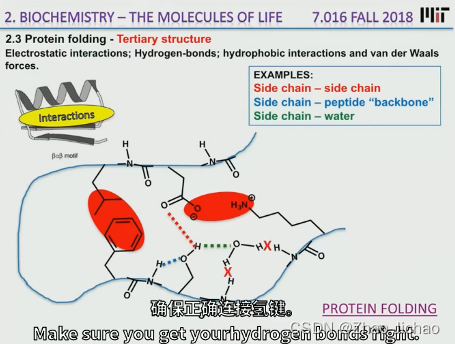
蛋白质的多肽链在各种二级结构的基础上再进一步盘曲或折迭形成具有一定规律的三维空间结构,称为蛋白质的三级结构(tertiary structure)。
蛋白质三级结构的稳定主要靠次级键,包括氢键、疏水键、盐键以及范德华力(Van der Waals force)等。这些次级键可存在于一级结构序号相隔很远的氨基酸残基的R基团之间,因此蛋白质的三级结构主要指氨基酸残基的侧链间的结合。次级键都是非共价键,易受环境中pH、温度、离子强度等的影响,有变动的可能性。二硫键不属于次级键,但在某些肽链中能使远隔的二个肽段联系在一起,这对于蛋白质三级结构的稳定上起着重要作用。
现也有认为蛋白质的三级结构是指蛋白质分子主链折叠盘曲形成构象的基础上,分子中的各个侧链所形成一定的构象。侧链构象主要是形成微区(或称结构域domain)。对球状蛋白质来说,形成疏水区和亲水区。亲水区多在蛋白质分子表面,由很多亲水侧链组成。疏水区多在分子内部,由疏水侧链集中构成,疏水区常形成一些“洞穴”或“口袋”,某些辅基就镶嵌其中,成为活性部位。
具备三级结构的蛋白质从其外形上看,有的细长(长轴比短轴大10倍以上),属于纤维状蛋白质(fibrous protein),如丝心蛋白;有的长短轴相差不多基本上呈球形,属于球状蛋白质(globular protein),如血浆清蛋白、球蛋白、肌红蛋白,球状蛋白的疏水基多聚集在分子的内部,而亲水基则多分布在分子表面,因而球状蛋白质是亲水的,更重要的是,多肽链经过如此盘曲后,可形成某些发挥生物学功能的特定区域,例如酶的活性中心等。
4. 四级结构 (quaternary structure)

具有二条或二条以上独立三级结构的多肽链组成的蛋白质,其多肽链间通过次级键相互组合而形成的空间结构称为蛋白质的四级结构(quarternary structure)。
其中,每个具有独立三级结构的多肽链单位称为 亚基 (subunit)。四级结构实际上是指亚基的立体排布、相互作用及接触部位的布局。亚基之间不含共价键,亚基间次级键的结合比二、三级结构疏松,因此在一定的条件下,四级结构的蛋白质可分离为其组成的亚基,而亚基本身构象仍可不变。
一种蛋白质中,亚基结构可以相同,也可不同。如烟草斑纹病毒的外壳蛋白是由2200个相同的亚基形成的多聚体;正常人血红蛋白A是两个α亚基与两个β亚基形成的四聚体;天冬氨酸氨甲酰基转移酶由六个调节亚基与六个催化亚基组成。有人将具有全套不同亚基的最小单位称为 原聚体 (protomer),如一个催化亚基与一个调节亚基结合成天冬氨酸氨甲酰基转移酶的原聚体。
某些蛋白质分子可进一步聚合成 聚合体 (polymer)。聚合体中的重复单位称为 单体 (monomer),聚合体可按其中所含单体的数量不同而分为 二聚体 (dimer)、三聚体 (trimer)、四聚体 (tetramer) … 寡/低聚体 (oligomer) 和 多聚体 (polymer) 而存在,如 胰岛素 (insulin) 在体内可形成二聚体及六聚体。








 蛋白质由氨基酸序列组成,其结构分为一级、二级、三级和四级结构。一级结构涉及氨基酸的线性排列,二级结构主要为α螺旋和β折叠,依赖氢键稳定。三级结构是多肽链的三维空间排列,四级结构涉及多条肽链间的交互作用。蛋白质的功能依赖于其精确的空间构象。
蛋白质由氨基酸序列组成,其结构分为一级、二级、三级和四级结构。一级结构涉及氨基酸的线性排列,二级结构主要为α螺旋和β折叠,依赖氢键稳定。三级结构是多肽链的三维空间排列,四级结构涉及多条肽链间的交互作用。蛋白质的功能依赖于其精确的空间构象。

















 1020
1020

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?










